

Roche şirketi tarafından Londra’daki UBS etkinliğinde bir sunum yapıldı. İsviçreli şirket tarafından etkinlikte çok sayıda hastalığa ve ilaca dair bilgiler paylaşıldı.
Sunumda SMA ilacı Risdiplan’la ilgili olarak şu noktalara değinildi:
- Ağızdan alınan ve etkili bir ilaç
- 1. tiplerdeki sonuçlar faydasını ispatlıyor.
- SMN proteinin hem omurilik sıvısında hem de çevre dokularda arttığı gözlendi.
- Güçlü güvenilirlik profiline sahiptir
- Şu ana kadar, çalışmaların geri çekilmesine sebep olacak hiçbir şey yaşanmadı.
- Denemeler geniş bir hasta grubu üstünde devam ediyor
- Bebeklerden ileri yaştaki yetişkinlere kadar
- 2. ve 3. tipler üzerinde ilacın denendiği çalışmanın sonuçları 2019’un sonlarında ayrıntılı olarak duyurulacak
- FDA ve EMA’ya başvurular yakında olacak
- 2019 yılı bitmeden ABD’de ve 2020 yılının ilk yarısında Avrupa’da ilgili kurumlara başvurulacak.
- Çok büyük bir pazar ve getiri potansiyeli taşıyor.
- İlk slayta buna değinilirken Risdiplam’ın bütün dünyadaki yıllık satış getirisinin 1 milyar İsviçre Frangı’nı ( yaklaşık 1 milyar dolar) aşacağı öngörülmüş.
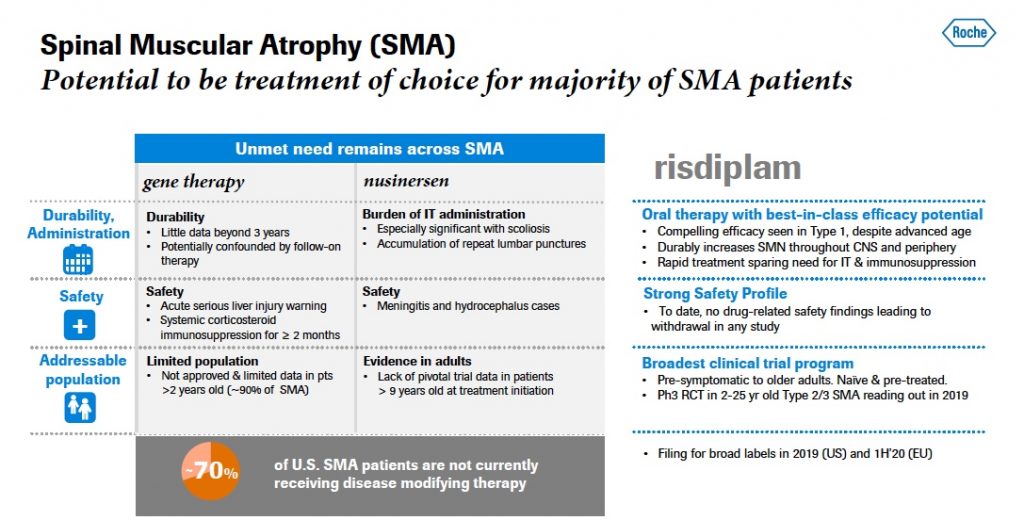
Spinraza ve Zolgensma ile Karşılaştırmalar
Sunumda Novartis’in gen tedavisi olan Zolgensma ve Spinraza’nın etken maddesi olan Nusinersen için şu eleştiriler getirildi:
- Zolgensma’nın eksileri
- 2 yaşın üstündeki hastalarda denendi ama henüz onaylanmadı. Sadece 2 yaşın altındaki hastalar için onaylandı, yani hastaların ancak %10’uan hitap edebiliyor.
- Karaciğer üzerinde yan etkileri var.
- Denemelerde 3 yılı geçen az veri bulunuyor.
- Spinraza’nın (Nusinersen) eksileri
- Uygulanması zor, özellikle skolyozu olan hastalarda çok zor
- Az da olsa hidrosefali vakaları gözlendi
- Denemelerde yetişkinler için çok fazla veri üretilememişti.
Roche şirketinin sunumunun tamamını okumak için tıklayınız.